摘要:研究揭示了慢性HBV感染中CD4+ Teff細(xì)胞通過(guò)CD40-CD40L軸激活肝臟庫(kù)普弗細(xì)胞(KCs),促使其分泌IL-12和IL-27,從而逆轉(zhuǎn)HBV特異性CD8+ T細(xì)胞功能衰竭的新機(jī)制。
慢性乙型肝炎病毒(HBV)感染影響著全球近3億人,其中相當(dāng)比例會(huì)發(fā)展為肝硬化和肝癌。病毒清除主要依賴CD8+細(xì)胞毒性T細(xì)胞的功能,但在慢性感染中,這些細(xì)胞往往陷入"功能衰竭"(exhaustion)狀態(tài)。尤其令人困惑的是,即使病毒抗原持續(xù)存在,為何有些患者能自發(fā)清除病毒?先前研究提示CD4+ T細(xì)胞的輔助功能可能至關(guān)重要,但其具體機(jī)制,特別是在肝臟這個(gè)特殊免疫微環(huán)境中的作用,始終是未解之謎。
意大利圣拉斐爾科學(xué)研究所在《Nature Immunology》發(fā)表的研究,通過(guò)構(gòu)建HBV特異性CD4+ TCR轉(zhuǎn)基因小鼠(Env126品系),結(jié)合多光子活體成像等先進(jìn)技術(shù),首次揭示了肝臟局部CD4+ T細(xì)胞與庫(kù)普弗細(xì)胞(KCs)的三元互動(dòng)機(jī)制。研究發(fā)現(xiàn),效應(yīng)性CD4+ T細(xì)胞(CD4+ Teff)通過(guò)CD40-CD40L分子直接激活KCs,促使后者分泌IL-12和IL-27。其中IL-12主要擴(kuò)增CD4+ T細(xì)胞池,而IL-27則是挽救CD8+ T細(xì)胞功能的關(guān)鍵因子。這一發(fā)現(xiàn)不僅解釋了肝臟局部免疫調(diào)控的特殊性,還為慢性乙肝的免疫治療提供了新思路。
 圖1 CD4+ T細(xì)胞允許庫(kù)普弗細(xì)胞逆轉(zhuǎn)肝細(xì)胞啟動(dòng)誘導(dǎo)的CD8+ T細(xì)胞功能障礙
圖1 CD4+ T細(xì)胞允許庫(kù)普弗細(xì)胞逆轉(zhuǎn)肝細(xì)胞啟動(dòng)誘導(dǎo)的CD8+ T細(xì)胞功能障礙關(guān)鍵技術(shù)包括:(1)構(gòu)建HBV Env126-138特異性CD4+ TCR轉(zhuǎn)基因小鼠;(2)采用rVSVEnv病毒載體在體激活T細(xì)胞;(3)多光子活體顯微技術(shù)觀察肝內(nèi)免疫突觸形成;(4)單細(xì)胞RNA測(cè)序分析T細(xì)胞亞群;(5)CLEC4f-iDTR-YFP小鼠進(jìn)行KCs特異性剔除;(6)慢性乙肝患者PBMCs體外培養(yǎng)驗(yàn)證IL-27的治療潛力。
CD4+ T細(xì)胞逆轉(zhuǎn)CD8+ T細(xì)胞功能障礙
通過(guò)共轉(zhuǎn)輸實(shí)驗(yàn)發(fā)現(xiàn),Env126 CD4+ Teff細(xì)胞不僅能預(yù)防還能逆轉(zhuǎn)由肝細(xì)胞抗原提呈誘導(dǎo)的CD8+ T細(xì)胞功能障礙。被"拯救"的CD8+ T細(xì)胞增殖能力增強(qiáng),抑制性受體(PD-1、Lag-3、CTLA-4)表達(dá)下降,同時(shí)效應(yīng)分子(IFNγ、TNF、Grzm-B)分泌增加。
抗原識(shí)別是關(guān)鍵而非表位連鎖
研究證實(shí)CD4+ T細(xì)胞的輔助作用需要直接抗原識(shí)別,但不需要與CD8+ T細(xì)胞識(shí)別的表位物理連接。在MHC-II缺陷小鼠中,CD4+ T細(xì)胞無(wú)法提供有效幫助,說(shuō)明TCR-MHC II相互作用不可或缺。
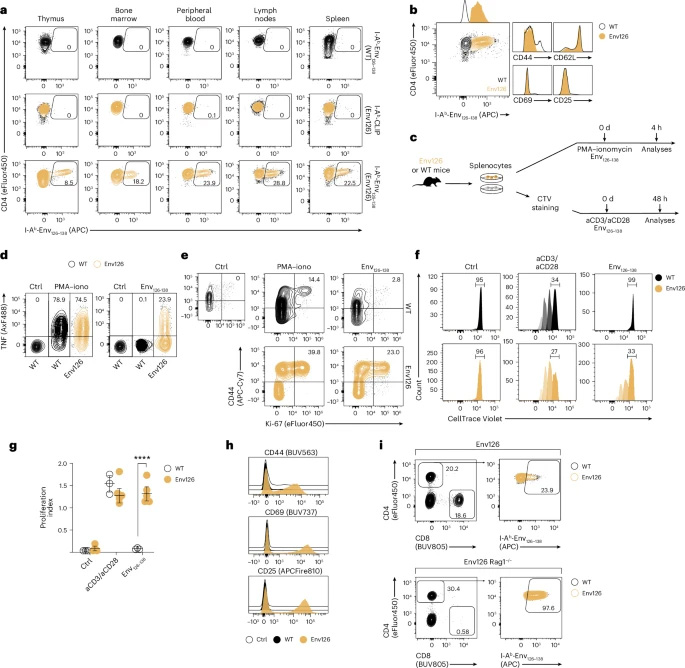
圖2 HBV特異性CD4+ TCR轉(zhuǎn)基因小鼠的構(gòu)建與表征
肝臟局部免疫突觸形成
通過(guò)阻斷淋巴細(xì)胞歸巢證明,CD4+ T細(xì)胞的輔助作用可不依賴次級(jí)淋巴器官,直接在肝臟內(nèi)完成。多光子成像捕捉到CD4+-CD8+-KCs三元穩(wěn)定互作結(jié)構(gòu),互作時(shí)間超過(guò)20分鐘,符合免疫突觸特征。
庫(kù)普弗細(xì)胞的核心作用
選擇性剔除實(shí)驗(yàn)顯示,KCs而非樹(shù)突狀細(xì)胞(DCs)是CD4+ T細(xì)胞發(fā)揮作用的關(guān)鍵平臺(tái)。被"許可"(licensed)的KCs高表達(dá)MHC II和共刺激分子(CD40、CD80、CD86),并分泌IL-27。
IL-27的治療潛力
在慢性乙肝患者中,外源性IL-27能顯著增強(qiáng)HBV特異性CD8+ T細(xì)胞反應(yīng),尤其對(duì)聚合酶特異性T細(xì)胞效果最顯著。這為臨床轉(zhuǎn)化提供了直接依據(jù)。
這項(xiàng)研究顛覆了傳統(tǒng)"三細(xì)胞"模型認(rèn)知,提出"肝內(nèi)許可"新范式:CD4+ Teff→KCs→CD8+ T細(xì)胞的級(jí)聯(lián)激活途徑。這不僅解釋了為何部分慢性感染者能自發(fā)控制病毒,更重要的是,IL-27作為可成藥靶點(diǎn),其臨床轉(zhuǎn)化風(fēng)險(xiǎn)較低,為開(kāi)發(fā)"功能性治愈"乙肝的新策略奠定了理論基礎(chǔ)。研究還暗示,類似機(jī)制可能存在于其他慢性病毒感染或腫瘤微環(huán)境中,為免疫治療研究開(kāi)辟了新方向。
參考資料
[1] CD4+ T cells license Kupffer cells to reverse CD8+ T cell dysfunction induced by hepatocellular priming
 蛋白酶K (源自林伯氏白色念球菌)
蛋白酶K (源自林伯氏白色念球菌) 茚三酮顯色溶液套裝,日立分析儀專用 (299-70501)
茚三酮顯色溶液套裝,日立分析儀專用 (299-70501) 氨基酸混合標(biāo)準(zhǔn)溶液,AN-2型 (011-14463)
氨基酸混合標(biāo)準(zhǔn)溶液,AN-2型 (011-14463) 表面潤(rùn)濕張力試驗(yàn)用混合液 Wetting Tension Test Mixture
表面潤(rùn)濕張力試驗(yàn)用混合液 Wetting Tension Test Mixture