摘要:新研究表明,用光和聲音刺激關鍵的大腦節律可以增加中間神經元的肽釋放。
麻省理工學院和其他地方的研究正在提供越來越多的證據,證明在40赫茲的伽馬腦節律頻率下,光的閃爍和聲音的滴答聲可以減少阿爾茨海默病(AD)的進展,并治療人類志愿者和實驗室老鼠的癥狀。在《自然》雜志上的一項新研究中,麻省理工學院Picower學習和記憶研究所的研究人員利用該疾病的小鼠模型揭示了一個可能有助于這些有益效果的關鍵機制:淀粉樣蛋白的清除,AD病理的標志,通過大腦的淋巴系統,一個最近發現的與大腦血管平行的“管道”網絡。
 圖1 多傳感器伽瑪刺激促進淋巴結清除淀粉樣蛋白
圖1 多傳感器伽瑪刺激促進淋巴結清除淀粉樣蛋白“自從我們在2016年公布了第一批結果以來,人們一直問我它是如何工作的?為什么是40赫茲?為什么不是其他的頻率呢? 這些確實是我們在實驗室里非常努力地解決的非常重要的問題。”該研究的資深作者Li-Huei Tsai說。
這篇新論文來自第一作者Mitch Murdock還是麻省理工學院(MIT)大腦與認知科學的博士生時的研究。實驗表明,當感覺伽馬刺激增加小鼠大腦中40赫茲的功率和同步性時,會促使一種特定類型的神經元釋放肽。研究結果進一步表明,這些短蛋白信號隨后驅動特定的過程,通過淋巴系統促進淀粉樣蛋白的清除。
“我們還沒有一個事件發生的確切順序的線性圖,但我們的實驗結果支持這種通過主要淋巴途徑清除的途徑。”Murdock說。
從伽瑪到淋巴細胞
因為先前的研究表明,淋巴系統是腦廢物清除的關鍵通道,可能受到腦節律的調節,Tsai和Murdock的團隊假設,這可能有助于解釋實驗室先前觀察到的伽馬感覺刺激降低了阿爾茨海默氏癥模型小鼠的淀粉樣蛋白水平。
Murdock等人用“5XFAD”小鼠進行實驗,這種小鼠是阿爾茨海默氏癥的基因模型,他們首先復制了實驗室之前的結果,即40赫茲的感官刺激增加了大腦中40赫茲的神經元活動,降低了淀粉樣蛋白水平。然后,他們開始測量通過淋巴系統攜帶廢物的液體是否有任何相關的變化。事實上,他們測量了與未治療的對照組相比,接受感覺伽馬刺激的小鼠腦組織中腦脊液的增加。他們還測量了腦組織間質液流出率的增加。此外,在接受伽瑪治療的小鼠中,他測量了排泄液體的淋巴管直徑的增加,并測量了頸淋巴結中淀粉樣蛋白積累的增加,頸淋巴結是血液流動的排泄部位。
為了研究這種增加的液體流動是如何發生的,研究小組把重點放在了星形膠質細胞的水通道蛋白4 (AQP4)上,它使細胞能夠促進淋巴液體交換。當他們用一種化學物質阻斷APQ4的功能時,就會阻止感覺刺激降低淀粉樣蛋白水平,從而阻止它改善小鼠的學習和記憶能力。作為一項額外的測試,他們使用了一種基因技術來破壞AQP4,這也干擾了γ驅動的淀粉樣蛋白清除。
除了星形膠質細胞中APQ4活性促進的液體交換外,伽馬波促進淋巴流動的另一種機制是通過增加鄰近血管的脈動。幾項測量顯示,與未治療的對照組相比,受到感覺伽馬刺激的小鼠動脈搏動更強。
跟蹤一種情況(如感覺伽馬刺激)如何影響不同細胞類型的最好的新技術之一是對它們的RNA進行測序,以跟蹤它們如何表達基因的變化。使用這種方法,Tsai和Murdock的團隊發現伽馬感覺刺激確實促進了與星形膠質細胞AQP4活性增加一致的變化。
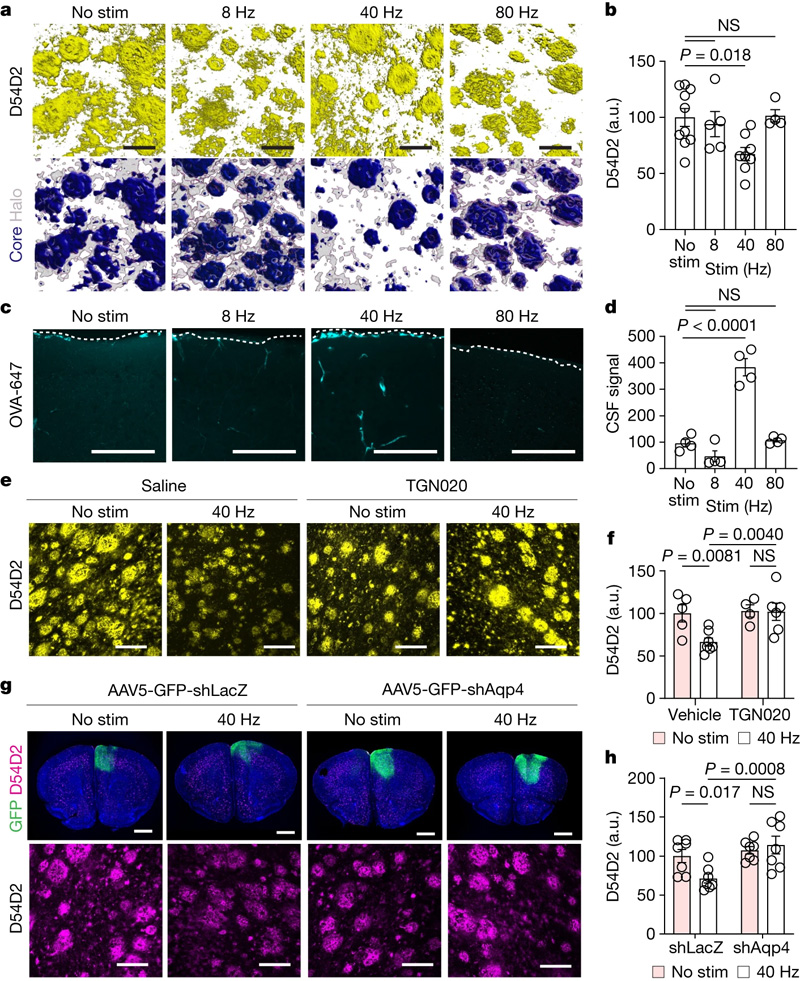 圖2 40 Hz多傳感器刺激促進AQP4依賴性清除淀粉樣蛋白
圖2 40 Hz多傳感器刺激促進AQP4依賴性清除淀粉樣蛋白多肽刺激
他們的研究表明,通過蛋白質攝入超過22%的日常飲食熱量會對負責清除細胞碎片的巨噬細胞產生負面影響,導致這些細胞在血管壁內堆積成“墓地”,并隨著時間的推移惡化動脈粥樣硬化斑塊。有趣的是,對循環氨基酸的分析表明,亮氨酸——一種在牛肉、雞蛋和牛奶等動物源性食物中富含的氨基酸——是異常巨噬細胞激活和動脈粥樣硬化風險的主要原因,這表明了個性化飲食調整或“精確營養”的進一步研究的潛在途徑。
導航蛋白質消費和心血管健康
RNA測序數據還顯示,在伽馬感覺刺激下,神經元的一個子集,稱為“中間神經元”,在幾種肽的產生上經歷了顯著的上升。這并不奇怪,因為已知肽的釋放依賴于腦節律頻率,但它仍然值得注意,因為一種特殊的肽,VIP,與阿爾茨海默氏癥的對抗有益,并有助于調節血管細胞,血液流動和淋巴清除。
抓住這個有趣的結果,研究小組進行了測試,發現伽馬治療小鼠大腦中的VIP增加了。研究人員還使用了肽釋放傳感器,觀察到感覺伽馬刺激導致表達vip的中間神經元的肽釋放增加。
但是這種γ刺激的肽釋放是否介導了淀粉樣蛋白的淋巴清除?為了找到答案,研究小組進行了另一項實驗:他們用化學方法關閉VIP神經元。當他們這樣做時,然后將小鼠暴露在感官伽馬刺激下,他們發現動脈搏動不再增加,伽馬刺激的淀粉樣蛋白也不再清除。
“我們認為有許多神經肽參與其中,”Murdock說。Tsai補充說,實驗室研究的一個主要新方向將是確定哪些肽或其他分子因素可能由感覺伽馬刺激驅動。
Tsai和Murdock補充說,雖然這篇論文關注的可能是一個重要的機制-淀粉樣蛋白的淋巴清除-通過感覺伽馬刺激幫助大腦,但它可能不是唯一重要的潛在機制。在這項研究中顯示的清除效果發生得相當快,但在實驗室實驗和臨床研究中,需要數周或數月的慢性感覺伽馬刺激才能對認知產生持續的影響。
然而,隨著每一項新的研究,科學家們對大腦節律的感官刺激如何有助于治療神經系統疾病有了更多的了解。
參考資料
[1] Multisensory gamma stimulation promotes glymphatic clearance of amyloid