摘要:蘇黎世大學的科學家們開發了一種創新的神經細胞培養模型,揭示了神經變性背后的復雜機制。
蘇黎世大學的科學家們開發了一種創新的神經細胞培養模型,揭示了神經變性背后的復雜機制。他們的研究確定了一種錯誤的蛋白質,作為治療肌萎縮側索硬化癥(ALS)和額顳葉癡呆(FTD)的有希望的治療靶點。
神經退行性疾病導致我們大腦中的一些神經元死亡,根據受影響的大腦區域導致不同的癥狀。在肌萎縮性側索硬化癥(ALS)中,運動皮層和脊髓中的神經元退化,導致癱瘓。另一方面,在額顳葉癡呆(FTD)中,位于大腦中與認知、語言和人格有關的部分的神經元受到影響。
 圖1 人類神經網絡模型揭示ALS和FTLD中的NPTX2病理
圖1 人類神經網絡模型揭示ALS和FTLD中的NPTX2病理ALS和FTD都是不斷發展的疾病,仍然缺乏有效的治療方法。隨著人口老齡化,與年齡相關的神經退行性疾病,如ALS和FTD的患病率預計將增加。
盡管在中樞神經系統神經元中發現了一種名為TDP-43的蛋白質的異常積累,這是絕大多數ALS和約一半的FTD患者的共同因素,但驅動神經退行性變的潛在細胞機制在很大程度上仍然未知。
靈活,耐用,可重復性:ALS和FTD研究的理想細胞培養模型
在他們的研究中,蘇黎世大學定量生物醫學院的第一作者Marian Hruska-Plochan和通訊作者Magdalini Polymenidou開發了一種新的神經細胞培養模型,該模型復制了神經元中TDP-43的異常行為。利用這個模型,他們發現NPTX2蛋白的毒性增加,表明它是ALS和FTD的潛在治療靶點。
為了模擬神經退化,Marian Hruska-Plochan開發了一種新的細胞培養模型,稱為“iNets”,來源于人類誘導多能干細胞。這些細胞起源于皮膚細胞,并在實驗室中被重新編程到非常早期的未分化階段,作為發展許多不同的,期望的細胞類型的來源。神經網絡是由相互連接的神經元和它們的支持細胞組成的網絡,這些細胞在培養皿中生長成多層。
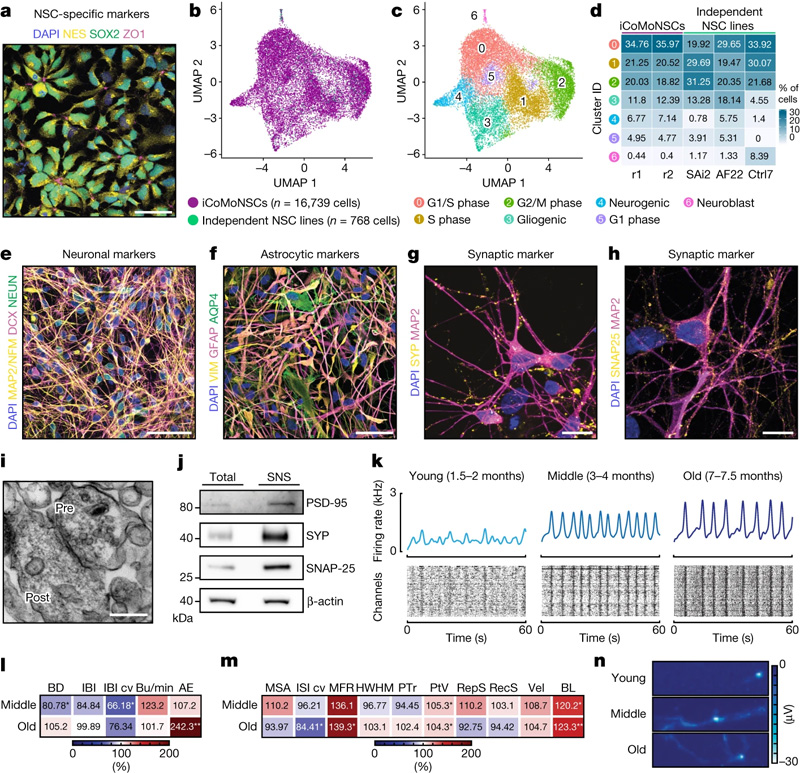 圖2 iCoMoNSC神經元形成功能網絡
圖2 iCoMoNSC神經元形成功能網絡這種培養持續的時間特別長——長達一年——而且很容易繁殖。“老化的神經網絡的健壯性使我們能夠進行原本不可能進行的實驗,”Hruska-Plochan說。“該模型的靈活性使其適用于各種實驗方法。”作為一個恰當的例子,iNets細胞培養為研究TDP-43功能障礙到神經退行性變的進展提供了理想的模型。
蛋白質功能障礙如何導致神經退行性變
利用inet模型,研究人員發現了NPTX2的毒性積累,這是一種通常由神經元通過突觸分泌的蛋白質,是TDP-43行為不當和神經元死亡之間缺失的一環。為了驗證他們的假設,他們檢查了已故ALS和FTD患者的腦組織,確實發現,同樣在患者中,NPTX2積聚在含有異常TDP-43的細胞中。這意味著iNets培養模型準確地預測了ALS和FTD患者的病理。
在inet模型的其他實驗中,研究人員測試了NPTX2是否可以成為治療ALS和FTD的藥物設計的靶點。該團隊設計了一個設置,當神經元遭受TDP-43行為不當時,他們降低了NPTX2的水平。他們發現,保持低水平的NPTX2可以抵消iNets神經元的神經變性。因此,減少NPTX2蛋白含量的藥物有可能成為阻止ALS和FTD患者神經退行性變的治療策略。
Magdalini Polymenidou看到了這一發現的巨大希望:“在將其應用于患者之前,我們還有很長的路要走,但NPTX2的發現給了我們一個明確的目標,即開發一種針對疾病核心的治療方法,”她說。她補充說:“結合其他研究小組最近確定的另外兩個靶點,可以想象,抗nptx2藥物可能在未來成為ALS和FTD聯合治療的關鍵組成部分。”
參考資料
[1] A model of human neural networks reveals NPTX2 pathology in ALS and FTLD
 |
 |
 |
| 官網:m.baichuan365.com |
微信服務號:iseebio |
微博:seebiobiotech |
 |
 |
 |
| 商城:mall.seebio.cn |
微信訂閱號:seebiotech |
泉養堂:www.canmedo.com |