摘要:研究人員詳細描述了炎癥信號分子IL-12導致阿爾茨海默病的確切機制。
研究人員來自柏林夏里特醫學院和馬克斯·德爾布呂克中心,他們詳細揭示了炎癥信號分子IL-12如何導致阿爾茨海默病的精確機制。該研究發表在《自然·衰老》雜志上。
大腦的免疫細胞——小膠質細胞,通常充當著盡職盡責的守護者。它們清除入侵者,如微生物,并清理細胞碎片——包括阿爾茨海默病特有的斑塊。然而,隨著大腦的衰老,小膠質細胞也會發生變化。雖然有些仍然能夠有效發揮作用,但另一些會逐漸失去保護作用,并開始分泌少量炎癥信號分子。
 圖1 白細胞介素-12信號通路通過破壞神經元與少突膠質細胞穩態驅動阿爾茨海默病病理進程
圖1 白細胞介素-12信號通路通過破壞神經元與少突膠質細胞穩態驅動阿爾茨海默病病理進程其中一種信號分子就是白細胞介素-12(IL-12)。通過細致的分析,由柏林夏里特醫學院神經病理學系主任弗蘭克·赫普納教授和馬克斯·德爾布呂克中心柏林醫學系統生物學研究所所長尼古拉·拉耶夫斯基教授領導的研究團隊,以及他們的合作伙伴,識別出IL-12如何觸發并加速阿爾茨海默病癡呆。他們的研究發表在《自然·衰老》上,可能會為新的聯合療法鋪平道路。
“數十年來,阿爾茨海默病的研究幾乎只專注于淀粉樣蛋白β和tau蛋白沉積,而炎癥被認為是一種副作用。”赫普納說,“直到最近,我們才開始認識到炎癥過程可能是疾病進展的主要驅動力。”2012年,赫普納的實驗室在《自然·醫學》雜志上報告稱,阻斷IL-12和IL-23顯著減少了小鼠大腦中與阿爾茨海默病相關的改變。“但我們無法用標準技術解開其背后的機制。”赫普納解釋道。他認為單細胞分析可能會提供更關鍵的線索,于是邀請拉耶夫斯基合作。
細胞在一生中會參考其遺傳指令來對外部刺激做出反應。研究人員利用單細胞分析來觀察這一過程,同時重建數千個單細胞中正在被讀取并轉化為蛋白質的基因。這些分析產生了海量數據集,如今可以借助人工智能和機器學習進行分析。然而,使用單細胞測序技術的一個主要挑戰是從組織樣本中分離單個細胞,而不損傷它們或導致意外變化。“在衰老的小鼠大腦中——尤其是那些有阿爾茨海默病斑塊的大腦——細胞緊密相連且糾纏不清,幾乎無法干凈地分離它們。”拉耶夫斯基解釋道。
他的團隊花了數年時間完善了一種變通方法。他們沒有分離整個細胞,而是從大腦組織中提取細胞核,并分析每個細胞中的RNA。通過與公開數據(如艾倫大腦圖譜)進行交叉比對,他們可以確保其方法能夠提供所有細胞群體的代表性快照。在本研究中,他們對超過8萬個細胞核的RNA進行了測序,并開發了專門的工作流程來處理數據。他們還重建了細胞之間的通信。“我們的團隊多次坐在一起試圖解讀這些極其復雜的數據。”拉耶夫斯基說,“這種早期的精心優化至關重要——沒有它,我們無法檢測到這些聯系。”
白細胞介素-12(IL-12)此前主要以其在克羅恩病和類風濕關節炎等自身免疫疾病中的作用而聞名,現在看來它在阿爾茨海默病的進展中也發揮著關鍵作用。它會損害兩種關鍵的腦細胞類型:成熟的少突膠質細胞,它們通常產生髓鞘——圍繞神經纖維的脂肪絕緣層,對快速信號傳導至關重要;以及中間神經元,這些神經元對認知和記憶尤其重要。IL-12與中間神經元結合會導致它們死亡。一個惡性循環開始了:隨著越來越多的小膠質細胞產生IL-12,越來越多的腦細胞受到損害。與此同時,仍然能夠正常發揮功能的小膠質細胞被清理額外細胞碎片的任務壓垮,因此無法清除阿爾茨海默病斑塊。
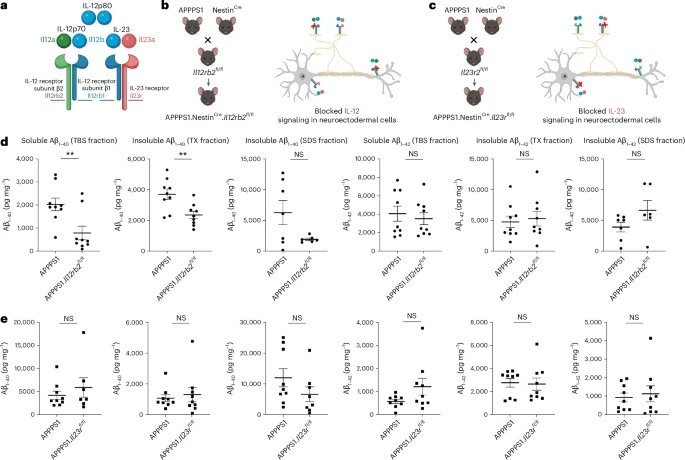 圖2 敲除IL-12特異性受體亞基IL12Rβ2可減少淀粉樣蛋白沉積負荷
圖2 敲除IL-12特異性受體亞基IL12Rβ2可減少淀粉樣蛋白沉積負荷為了驗證這一機制,研究人員在小鼠和人類組織中進行了測試。當赫普納的團隊在細胞培養和小鼠模型中阻斷IL-12時,他們能夠阻止與疾病相關的改變。在哥廷根的馬普多學科科學研究所拍攝的小鼠大腦組織的電子顯微照片也顯示了髓鞘結構和神經纖維密度如何根據IL-12信號通路是否存在而發生變化。在蘇黎世大學進行的質譜分析(脂質組學)證實了脂肪絕緣層成分的改變。對阿爾茨海默病患者尸檢組織的研究進一步證實了這些結果——疾病越嚴重,組織中IL-12的含量就越高。含有人類少突膠質細胞的細胞培養對IL-12也非常敏感。
“我們現在對這一機制有了非常詳細的了解,單細胞技術是關鍵的催化劑。唯一剩下的問題是IL-12首先影響哪種細胞類型——少突膠質細胞、中間神經元,還是兩者同時?”赫普納說,他也是德國神經退行性疾病研究中心的神經免疫學小組負責人。
該研究具有直接的臨床意義,因為已經有藥物可以阻斷IL-12。研究人員希望臨床醫生能夠在此基礎上開展臨床試驗。“如果這些藥物被證明有效,它們將成為我們對抗阿爾茨海默病的新武器。阿爾茨海默病并非只有一個原因。疾病的一個軸至少在某些患者中由免疫系統控制。減緩神經退行性變需要聯合療法。”赫普納強調。這種療法可以在疾病早期開始,因為IL-12可以在血液或腦脊液中檢測到。
與此同時,夏里特和馬克斯·德爾布呂克中心的團隊正在探索一個新的假設:大腦中的微塑料是否會導致小膠質細胞產生IL-12?“小膠質細胞可能難以處理微塑料,從而引發炎癥反應。”拉耶夫斯基表示,“這可能會揭示環境因素與廣泛疾病之間的聯系。”盡管尚未得到證實,但兩個團隊都認為這是一個引人入勝且重要的研究方向。
參考資料
[1] Interleukin-12 signaling drives Alzheimer’s disease pathology through disrupting neuronal and oligodendrocyte homeostasis
 |
 |
 |
| 官網:m.baichuan365.com |
微信服務號:iseebio |
微博:seebiobiotech |
 |
 |
 |
| 商城:mall.seebio.cn |
微信訂閱號:seebiotech |
泉養堂:www.canmedo.com |
 圖1 白細胞介素-12信號通路通過破壞神經元與少突膠質細胞穩態驅動阿爾茨海默病病理進程
圖1 白細胞介素-12信號通路通過破壞神經元與少突膠質細胞穩態驅動阿爾茨海默病病理進程