【外泌體科普1】什么是外泌體?

|
[1]
|
Kowal J, et al. (2016) Proteomic comparison defines novel markers to characterize heterogeneous populations of extracellular vesicle subtypes. Proc Natl Acad Sci U S A, 113 (8) : E968-977.
|
|
[2]
|
Colombo M, Raposo G, & Thery C (2014) Biogenesis, secretion, and intercellular interactions of exosomes and other extracellular vesicles. Annu Rev Cell Dev Biol, 30 : 255-289.
|
|
[3]
|
Bobrie A, Colombo M, Raposo G, & Thery C (2011) Exosome secretion : molecular mechanisms and roles in immune responses. Traffic, 12 (12) : 1659-1668.
|
|
[4]
|
Bahrini I, Song JH, Diez D, & Hanayama R (2015) Neuronal exosomes facilitate synaptic pruning by up-regulating complement factors in microglia. Sci Rep, 5 : 7989.
|
|
[5]
|
Kramer-Albers EM & Hill AF (2016) Extracellular vesicles: interneural shuttles of complex messages. Curr Opin Neurobiol, 39 : 101-107.
|
|
[6]
|
Tkach M & Thery C (2016) Communication by Extracellular Vesicles : Where We Are and Where We Need to Go. Cell, 164 (6) : 1226-1232.
|
|
[7]
|
Hoshino A, et al. (2015) Tumour exosome integrins determine organotropic metastasis. Nature, 527 (7578): 329-335.
|
|
[8]
|
Thomou T, et al. (2017) Adipose-derived circulating miRNAs regulate gene expression in other tissues. Nature, 542 (7642) : 450-455.
|
|
[9]
|
Izquierdo-Useros N, Puertas MC, Borras FE, Blanco J, & Martinez-Picado J (2011)Exosomes and retroviruses : the chicken or the egg? Cell Microbiol, 13 (1) : 10-17.
|
|
[10]
|
Regev-Rudzki N, et al. (2013) Cell-cell communication between malaria-infected red blood cells via exosome-like vesicles. Cell, 153 (5) : 1120-1133.
|
|
[11]
|
Valadi H, et al. (2007) Exosome-mediated transfer of mRNAs and microRNAs is a novel mechanism of genetic exchange between cells. Nat Cell Biol, 9 (6) : 654-659.
|
|
[12]
|
Geiger A, Walker A, & Nissen E (2015) Human fibrocyte-derived exosomes accelerate wound healing in genetically diabetic mice. Biochem Biophys Res Commun, 467 (2) : 303-309.
|
|
[13]
|
Bell BM, Kirk ID, Hiltbrunner S, Gabrielsson S, & Bultema JJ (2016) Designer exosomes as next-generation cancer immunotherapy. Nanomedicine, 12 (1) : 163-169.
|
|
[14]
|
Zhang HG, et al. (2006) A membrane form of TNF-alpha presented by exosomes delays T cell activation-induced cell death. J Immunol, 176 (12) : 7385-7393.
|
|
[15]
|
Batrakova EV & Kim MS (2015) Using exosomes, naturally-equipped nanocarriers, for drug delivery. J Control Release, 219 : 396-405.
|
|
[16]
|
Thind A & Wilson C (2016) Exosomal miRNAs as cancer biomarkers and therapeutic targets. J Extracell Vesicles, 5 : 31292.
|
|
[17]
|
Nakai W, et al. (2016) A novel affinity-based method for the isolation of highly purified extracellular vesicles. Sci Rep, 6 : 33935.
|
|
[18]
|
Witwer KW, et al. (2013) Standardization of sample collection, isolation and analysis methods in extracellular vesicle research. J Extracell Vesicles, 2.
|
|
[19]
|
Lotvall J, et al. (2014) Minimal experimental requirements for definition of extracellular vesicles and their functions : a position statement from the International Society for Extracellular Vesicles. J Extracell Vesicles, 3 : 26913.
|
|
[20]
|
Consortium E-T, et al. (2017) EV-TRACK : transparent reporting and centralizing knowledge in extracellular vesicle research. Nat Methods, 14 (3) : 228-232.
|
華山 力成
 |
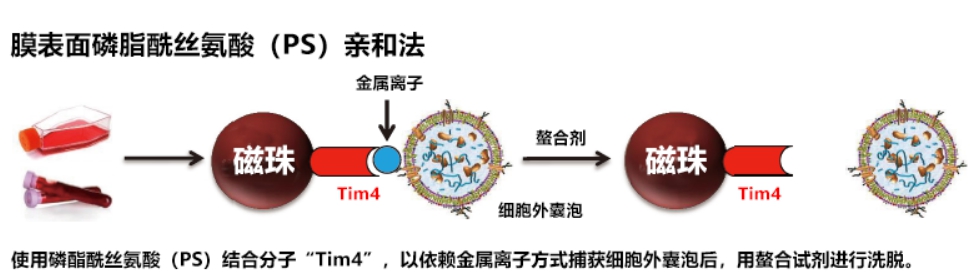
【特點(diǎn)】
● 可提取高純度的完整外泌體
● 可從血清、血漿、尿液等樣品中提取外泌體
● 重復(fù)性高,回收量穩(wěn)定
● 操作簡單,可處理多個(gè)樣品(無需超速離心)
|
|||||
|
【產(chǎn)品列表】
|
|
[1]
|
Tkach, M. et al. Communication by Extracellular Vesicles : Where We Are and Where We Need to Go. Cell 164, 1226-1232 (2016).
|
|
[2]
|
Raimondo, F. et al. Advances in membranous vesicle and exosome proteomics improving biological understanding and biomarker discovery. Proteomics 11, 709-720 (2011).
|
|
[3]
|
Trajkovic, K. et al. Ceramide triggers budding of exosome vesicles into multivesicular endosomes. Science 319 (5867) : 1244–7 (2008).
|
|
[4]
|
Miyanishi, M. et al. Identification of Tim4 as a phosphatidylserine receptor. Nature 450, 435-439 (2007).
|
|
[5]
|
Nakai, W. et al. A novel affinity-based method for the isolation of highly purified extracellular vesicles. Sci. Rep. 6, 33935 (2016).
|
 |
 |
 |
| 官網(wǎng):m.baichuan365.com | 微信服務(wù)號(hào):iseebio | 微博:seebiobiotech |
 |
 |
 |
| 商城:mall.seebio.cn | 微信訂閱號(hào):seebiotech | 泉養(yǎng)堂:www.canmedo.com |
相關(guān)資訊
- 新研究在干細(xì)胞中找到“不老之泉”的奧秘
- FDA批準(zhǔn)首個(gè)非小細(xì)胞肺癌(NSCLC)血液樣本基因檢測試劑盒
- 永攀高峰、閃耀未來|西寶6月銷售榜首、沖刺先鋒、杰出服務(wù)獎(jiǎng)揭曉
- FSI Genetics:新工具可從未知個(gè)體的DNA片段預(yù)測出該個(gè)體的眼睛、毛發(fā)和皮膚顏色!
- 哈佛醫(yī)學(xué)院主動(dòng)撤回31篇心臟干細(xì)胞文章
- 重磅!科學(xué)家完成對66種癌癥類型中2.8萬份腫瘤樣本的基因組分析 識(shí)別出568個(gè)癌癥驅(qū)動(dòng)基因!
- Cell:將飲食和腸道微生物結(jié)合起來預(yù)防胃腸道疾病
- 苯甲基樹突聚合物
- 中美科學(xué)家揭示骨生成新機(jī)制
- 抗真菌蛋白DECTIN-1可用于自身免疫疾病和癌癥治療
新進(jìn)產(chǎn)品
同類文章排行
- 重組胰蛋白酶(RTrypsin)
- 測序級(jí)重組賴氨酰內(nèi)肽酶/胰蛋白酶預(yù)混裝
- 胰蛋白酶,豬胰腺來源,質(zhì)譜等級(jí)
- 測序級(jí)重組胰蛋白酶MTrypsin
- BIOMOL(R) Green
- 單/多聚泛素化偶聯(lián)物單克隆抗體(UBCJ2)
- 來自昆蟲培養(yǎng)細(xì)胞的無細(xì)胞蛋白質(zhì)合成試劑盒 Transdirect insect cell
- PUREfrex(R) 2.0 PUREfrex(R) 酶無細(xì)胞蛋白合成試劑盒
- PUREfrex(R) 定制試劑盒
- 非天然氨基酸
資訊文章
您的瀏覽歷史