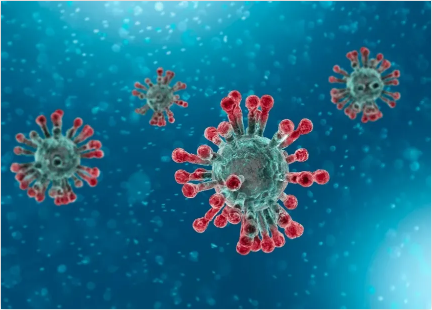
近日,葛蘭素史克(GSK)與Vir生物技術公司聯合宣布,已向美國食品藥品監督管理局(FDA)提交了單抗藥物VIR-7831(GSK4182136)的緊急使用授權(EUA),擬用于治療12歲以上(40公斤以內)可能存在住院或死亡風險的輕度或中度COVID-19患者。
據GSK和Vir公布的資料顯示,VIR-7831是一種具有雙重作用的SARS-CoV-2單克隆抗體,該抗體基于Xencor的Xtend™技術,既能阻斷病毒入侵健康細胞,又能清除感染細胞。
一項發表在國際期刊《bioRxiv》上的研究指出,與其他單克隆抗體相比,VIR-7831 可與 SARS-CoV-2 棘狀蛋白(spike protein)的高度保守表位結合,有效對抗英國、南非和巴西的新冠病毒(SARS-CoV-2)變異體,避免機體產生耐藥性。
今年3月,鑒于VIR-7831 的療效顯著,獨立數據監測委員會(Independent Data Monitoring Committee, IDMC)建議應盡早終止該藥的Ⅲ期臨床試驗,以便將該藥盡快用于COVID-19患者的治療。與此同時,葛蘭素史克(GSK)與Vir生物技術公司將以Ⅲ期臨床試驗數據為基礎,向美國食品藥品監督管理局(FDA)提交生物制品許可申請(BLA)。
值得一提的是,禮來和再生元制藥(Regeneron)的COVID-19“抗體雞尾酒療法”早在去年11月份就獲得了美國食品藥品監督管理局的緊急使用授權,但美國官員透露,由于該療法需要在患者出現癥狀的短時間內靜脈注射才能有效,因此未能在市場上廣泛普及。
目前,盡管VIR-7831的研究進展落后于禮來和再生元制藥(Regeneron)的“抗體雞尾酒療法”,但GSK和Vir表示,計劃將于今年第二季度開展兩項新的Ⅲ期臨床試驗COMET-TAIL和COMET-STAR,一方面評估VIR-7831是否會降低COVID-19高風險成年患者的住院率或死亡率,另一方面評估高風險未感染成年人在接受VIR-7831干預后,是否能預防COVID-19的發生。
未來,GSK和Vir將繼續與歐洲藥品管理局(EMA)以及全球其他監管機構進行討論,以便盡快為推進VIR-7831的上市。
 |
 |
 |
| 官網:m.baichuan365.com |
微信服務號:iseebio |
微博:seebiobiotech |
 |
 |
 |
| 商城:mall.seebio.cn |
微信訂閱號:seebiotech |
泉養堂:www.canmedo.com |