劍橋大學(xué):青光眼藥物可能有助于預(yù)防阿爾茨海默病相關(guān)的tau蛋白積聚

圖1 碳酸酐酶抑制通過增強(qiáng)tau蛋白分泌改善tau蛋白毒性
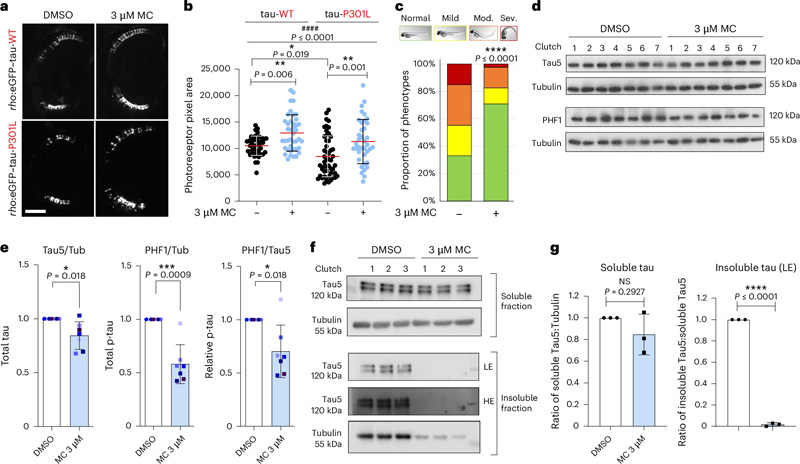
圖2 甲氧卡巴醇改善了斑馬魚模型中tau誘導(dǎo)的毒性,并降低了過度磷酸化和不溶性tau水平
 |
 |
 |
| 官網(wǎng):m.baichuan365.com | 微信服務(wù)號(hào):iseebio | 微博:seebiobiotech |
 |
 |
 |
| 商城:mall.seebio.cn | 微信訂閱號(hào):seebiotech | 泉養(yǎng)堂:www.canmedo.com |
相關(guān)資訊
- 震驚!哈佛大學(xué)超7萬樣本研究:麻腮風(fēng)和百白破疫苗竟能對(duì)重癥新冠患者提供保護(hù)!
- 槐糖脂:綠色生物表面活性劑多重功效及應(yīng)用
- 長期熬夜會(huì)猝死?心臟晝夜節(jié)律需關(guān)注
- 突破!中山大學(xué)舒躍龍團(tuán)隊(duì)首次發(fā)現(xiàn),MX1罕見變異增加人類對(duì)H7N9病毒易感性
- Seebio西寶生物產(chǎn)品品牌介紹
- PD-1 (human) ELISA Kit;PD-1 (人) ELISA試劑盒
- 軟骨素/皮膚素硫酸鹽雙糖標(biāo)準(zhǔn)品
- Protein G親和介質(zhì)——層析介質(zhì)優(yōu)選西寶生物
- 自然-通訊:利用CRISPR將皮膚細(xì)胞轉(zhuǎn)變?yōu)槎嗄芨杉?xì)胞
- 女神節(jié)|請(qǐng)接收西寶的“寵愛”
新進(jìn)產(chǎn)品
同類文章排行
- 劍橋大學(xué):青光眼藥物可能有助于預(yù)防阿爾茨海默病相關(guān)的tau蛋白積聚
- 《Cell》與帕金森病相關(guān)的蛋白質(zhì)聚集的新機(jī)制
- Nature子刊:首次揭示肝炎和腎損傷之間的聯(lián)系
- 《自然》:突變的RAS開關(guān)在癌癥中沒有斷裂,而只是有缺陷
- Cell子刊:暴飲暴食如何導(dǎo)致糖尿病?神經(jīng)遞質(zhì)激增
- 《Cell》癌細(xì)胞逃避免疫反應(yīng)新機(jī)制被發(fā)現(xiàn)了:它們能抑制核糖體功能
- NEJM:首次發(fā)現(xiàn)lncRNA基因缺失引起神經(jīng)發(fā)育疾病
- 干細(xì)胞移植會(huì)增加癌癥風(fēng)險(xiǎn)嗎?
- Science:有益的腸道微生物具有驚人的代謝能力!
- Nature:免疫療法阻斷瘢痕形成,改善心力衰竭小鼠的心臟功能
資訊文章
您的瀏覽歷史