摘要:開發(fā)出了首個(gè)基于mRNA的疫苗,其或能100%有效抵御一種對人類致死的細(xì)菌。
信使RNA(mRNA)脂質(zhì)納米顆粒(LNP)疫苗如今已經(jīng)成為一種有效的疫苗接種策略,盡管目前其適用于病毒性病原體,但有關(guān)該平臺(tái)抵御細(xì)菌病原體有效性的數(shù)據(jù)卻非常有限。
近日,一篇發(fā)表在國際雜志Science Advances上題為“A single-dose F1-based mRNA-LNP vaccine provides protection against the lethal plague bacterium”的研究報(bào)告中,來自以色列特拉維夫大學(xué)等機(jī)構(gòu)的科學(xué)家們通過研究開發(fā)出了首個(gè)基于mRNA的疫苗,其或能100%有效抵御一種對人類致死的細(xì)菌。
 圖1 科學(xué)家們通過研究開發(fā)出了首個(gè)基于mRNA的疫苗
圖1 科學(xué)家們通過研究開發(fā)出了首個(gè)基于mRNA的疫苗通過對動(dòng)物模型進(jìn)行研究,研究人員發(fā)現(xiàn),所有接受治療的動(dòng)物都能被保護(hù)抵御細(xì)菌(鼠疫耶爾森菌)的感染,這種新型技術(shù)或能幫助快速開發(fā)出針對細(xì)菌性疾病的有效疫苗,包括對抗生素耐藥的細(xì)菌所引起的疾病。
研究者Edo Kon解釋道,到目前為止,mRNA疫苗(比如針對COVID-19的mRNA疫苗)被認(rèn)為對于抵御病毒感染有效,但卻對細(xì)菌感染沒有作用;然而這類疫苗的最大優(yōu)勢除了其有效性之外,就是其能非常快速地被開發(fā)出來,一旦諸如SARS-CoV-2病毒的遺傳序列被公布,研究人員僅需要花費(fèi)63天時(shí)間就能開始首次臨床試驗(yàn);然而,直到現(xiàn)在,研究人員認(rèn)為,抵御細(xì)菌感染的mRNA疫苗從生物學(xué)上來講是無法實(shí)現(xiàn)的。這項(xiàng)研究中,研究人員就通過研究開發(fā)了針對致死性細(xì)菌的100%有效的mRNA疫苗。
研究人員解釋道,病毒會(huì)依賴于宿主細(xì)胞來進(jìn)行繁殖,將其自身的mRNA分子插入到人類細(xì)胞中,病毒既能利用我們的細(xì)胞作為工廠來生產(chǎn)基于自身遺傳物質(zhì)的病毒蛋白,從而復(fù)制自己。在mRNA疫苗中,這種相同的分子能在實(shí)驗(yàn)室中被合成,隨后就能包裹到類似人類細(xì)胞膜的脂質(zhì)納米顆粒中,當(dāng)疫苗注射到人體后,脂質(zhì)就會(huì)粘附到細(xì)胞上,隨后細(xì)胞就會(huì)產(chǎn)生病毒蛋白,當(dāng)免疫系統(tǒng)熟悉了這些蛋白后,其就會(huì)學(xué)習(xí)在接觸到真實(shí)病毒時(shí)如何保護(hù)機(jī)體自身了。
由于病毒會(huì)在我們自身的細(xì)胞中制造蛋白質(zhì),從病毒遺傳序列所翻譯出的蛋白質(zhì)與從實(shí)驗(yàn)室中合成的mRNA所翻譯的蛋白質(zhì)相似;然而,細(xì)菌或許就是一個(gè)完全不同的故事,其并不需要宿主自身的細(xì)胞來產(chǎn)生自身的蛋白質(zhì),而且,由于人類和細(xì)菌的進(jìn)化過程并不相同,因此細(xì)菌所產(chǎn)生的蛋白質(zhì)就與人類細(xì)胞所產(chǎn)生的蛋白質(zhì)不同,即使是基于相同的遺傳序列也是如此。
為此研究人員就嘗試在人類細(xì)胞中合成細(xì)菌蛋白,但暴露于這些蛋白質(zhì)會(huì)導(dǎo)致機(jī)體出現(xiàn)較低的抗體水平且普遍缺乏保護(hù)性免疫反應(yīng),這或許是因?yàn)椋M管細(xì)菌所產(chǎn)生的蛋白質(zhì)從本質(zhì)上來講與在實(shí)驗(yàn)室中合成的蛋白質(zhì)基本相同,且都是基于相同的“制造指令”,但在人體細(xì)胞中所產(chǎn)生的蛋白質(zhì)在從人體細(xì)胞分泌時(shí)就會(huì)發(fā)生重大變化,比如會(huì)增加糖類分子的水平等。
為了解決這個(gè)問題,研究人員開發(fā)出了分泌細(xì)菌蛋白的方法,同時(shí)還繞過了經(jīng)典的分泌途徑,這一途徑在這種應(yīng)用中是最容易出現(xiàn)問題的,其結(jié)果就是會(huì)產(chǎn)生顯著的免疫反應(yīng),免疫系統(tǒng)會(huì)將疫苗中的蛋白質(zhì)視為免疫原性細(xì)菌蛋白,為了增強(qiáng)細(xì)菌蛋白的穩(wěn)定性并確保其在體內(nèi)不會(huì)被快速分解,研究人員利用一部分人類蛋白對其加固,通過結(jié)合兩種突破性的策略,研究人員就能獲得全面的免疫反應(yīng)。
Peer教授說道,目前有很多致病菌我們并沒有疫苗,此外,由于人們在過去幾十年里過量使用抗生素,很多細(xì)菌都對抗生素產(chǎn)生了一定的耐受性,因此,抗生素耐藥菌已經(jīng)對全球人類的健康構(gòu)成了嚴(yán)重的威脅,因此開發(fā)一種新型疫苗或許就能為改善人類健康提供一定的基礎(chǔ)。
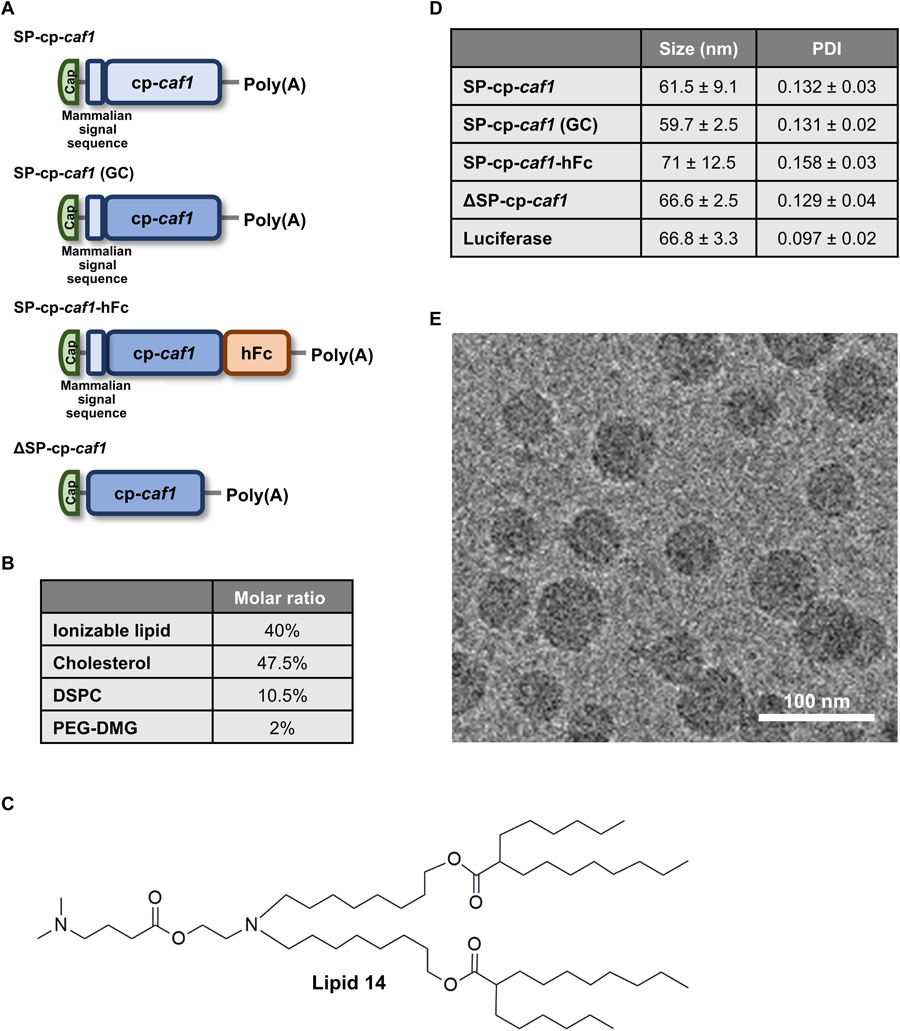 圖2 整個(gè)研究中使用的mRNA-LNPs制劑的結(jié)構(gòu)設(shè)計(jì)、物理化學(xué)特性以及SP-cp-caf1 mRNA-LNPs引起的免疫反應(yīng)。
圖2 整個(gè)研究中使用的mRNA-LNPs制劑的結(jié)構(gòu)設(shè)計(jì)、物理化學(xué)特性以及SP-cp-caf1 mRNA-LNPs引起的免疫反應(yīng)。這項(xiàng)研究中,研究人員檢測了新型的mRNA疫苗在治療被致死性細(xì)菌感染的動(dòng)物中的作用效果,在一周內(nèi)所有未接種疫苗的動(dòng)物都死亡了,而接種了新型疫苗的動(dòng)物則生存良好;此外,在其中一種疫苗策略中,但一個(gè)劑量的疫苗在使用兩周后就能為動(dòng)物機(jī)體提供全面的保護(hù)力,僅需要一劑疫苗就能提供全面保護(hù)的能力對于抵御未來快速擴(kuò)散的細(xì)菌的流行和爆發(fā)至關(guān)重要。
值得注意的是,COVID-19疫苗之所以能被很快地開發(fā)出來因?yàn)槠湟蕾囉诳茖W(xué)家們針對相類似病毒的mRNA疫苗多年的研究,如果明天我們面臨某種細(xì)菌的大流行,我們的研究或許就能為快速開發(fā)安全且有效的mRNA疫苗提供新的路徑。
綜上,本文研究結(jié)果表明,這種新型的mRNA-LNP疫苗或能在C57BL/6小鼠中產(chǎn)生體液和細(xì)胞免疫反應(yīng),并在單劑量注射后能提供抵御鼠疫耶爾森菌的快速全面的保護(hù),相關(guān)研究結(jié)果或?yàn)殚_發(fā)急需有效的抗菌疫苗開辟了新的路徑。
參考資料:
[1] A single-dose F1-based mRNA-LNP vaccine provides protection against the lethal plague bacterium